Scheikunde
Opdracht: Het atoommodel van Rutherford (1,2,3)
Voorwoord;
Bij deze opdracht moeten we 3 vragen gaan onderzoeken, en op minimaal 1 A4 verwoorden. We gaan eerst uitleggen wie Rutherford nou precies is.
Wie is Rutherford?
Rutherford is een scheikundige, geboren in 1899. Er zijn nog een paar scheikundige voor Rutherford geweest die ook het atoommodel bestudeerde.
Rutherford experimenteerde met het model van Thomson .Hij kwam erachter dat sommige stoffen deeltjes afstootte (straling). Zijn experiment was niet zo vreemd, aangezien het al een paar keer was uitgevoerd. Maar Rutherford liet het er niet bij liggen en onderzocht verder.
Waarom verwachtte Rutherford dat de alfadeeltjes rechtdoor zouden gaan?
Rutherford schiet met alfadeeltjes op goudfolie en ontdekt de atoomkern: zeer klein, zwaar en positief geladen. Alfadeeltjes zijn heliumkernen.
Hiernaast zie je wat Rutherford verwachtte dat er zou gebeuren. Hij dacht dat ze recht door het goud folie zouden gaan. Deze verwachtingen klopte echter niet.
Omdat een deel van deze alfadeeltjes er niet doorheen ging maar terugkaatste, was de gedacht van Rutherford fout. Dit komt omdat er bekend is dat de alfadeeltjes veel zwaarder zijn dan de elektronen. Na verder onderzoek kwam Rutherford erachter, er cirkelen negatieve elektronen rond de positieve kern. Die positieve kern zorgde ervoor dat positieve zware alfadeeltjes werden teruggekaatst, en er niet doorheen gingen.
Dit zijn er 1 op de 8000,want negatieve deeltje stoten positieve deeltjes af.
Later kwam Rutherford erachter dat rond die kern ook nog neutralen aanwezig waren, neutralen zijn niet geladen.
Rutherford wist dus nog niks af van de negatieve deeltjes rond de positieve kern. Want als de kern alleen maar positief was, zou er ook niks teruggekaatst worden, omdat er geen positieve deeltjes zijn die de negatieve deeltjes afstoten.
Na deze ontdekking maakt Rutherford zijn atoommodel.
Het atoom bestaat uit heel lichte negatieve elektronen rond een kleine zware positieve kern.
Welke gegeven leidde Rutherford af uit zijn experiment?
Als de atomen bollen met positieve lading zouden zijn, met negatieve elektronen daarin, dan zouden de krachten op een geladen deeltje elkaar steeds grotendeels combineren, en zouden alleen kleine bochten mogelijk zijn. Uit de experimenten leidde Rutherford af dat de positieve ladingdragers in het atoom zwaar moeten zijn in een volume dat veel kleiner is dan de omvang van het atoom, dit terwijl er maar een zeer klein deel van de straling weerkaatst werd.
Dit kleine deel van het atoom moet dus ook het overgrote deel van de massa bevatten. En hier draaien dan de lichte elektronen omheen. Zo ontstond dus het beeld van het atoom als een klein zonnestelsel.
De elektronen worden in hun banen gehouden door de aantrekkende kracht van de kernlading, zoals de aantrekkende zwaartekracht van de zon dat doet met de planten. Net zoals het zonnestelsel, bestaat het atoom voornamelijk uit lege ruimte.
Hoe ziet het atoommodel volgens Rutherford eruit?
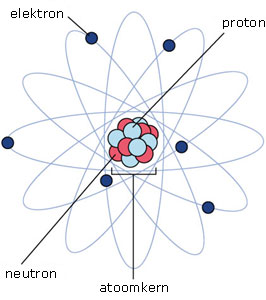
 Op basis van de bovenstaande experimenten stelde Rutherford een atoommodel op, waarbij hij het atoom omschreef als een positief geladen kern van protonen met daaromheen een wolk van elektronen in een verdunde ruimte.
Op basis van de bovenstaande experimenten stelde Rutherford een atoommodel op, waarbij hij het atoom omschreef als een positief geladen kern van protonen met daaromheen een wolk van elektronen in een verdunde ruimte.





REACTIES
1 seconde geleden